
授权合作(License):License是近年来制药领域非常流行的一种产品引入方式,其含义是指:产品引入方通过向产品授权方支付一定首付款,并约定后续的里程碑款项及未来的销售提成,从而获得在某些特定国家地区的研发、生产和销售的商业化权利。
中国目前的医药行业与10年前大为不同,最大的区别在于从渠道为王向品种为王的转变,“牛品种”成为市场追逐的热点。体现在资本市场上,就是估值体系从PEG向PEG+Pipeline的转变。净利润不再是支撑估值的唯一因素,研发管线丰富的公司,即使公司亏损甚至没有收入,依然可以获得资本市场很高的估值认可,并且具备在香港或者科创板上市的通路。
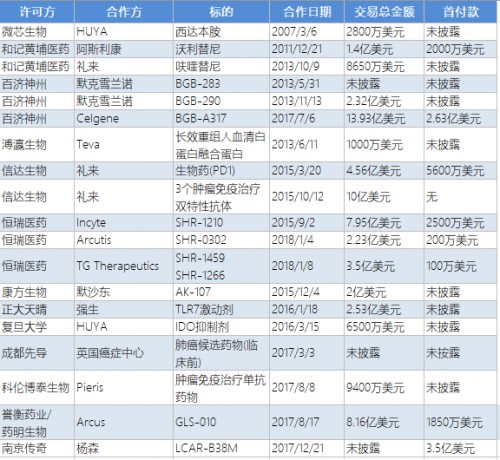
依据引入方向不同,授权合作可以分为License-in和License-out两类,前者是引入方付费向授权方购买许可,后者是授权方收费向引入方授予许可。在中国新药研发领域,近年来License-in和License-out都比较常见,相对而言,License-out是要求中国的研发标的得到国际巨头企业的认可,难度要更大。目前,中国制药企业License-in进海外品种已经很多了,尤其是再鼎医药将License-in模式系统化以后,这一类合作已经数量众多。而License-out的数量还相对少,下表列出部分中国产品License-out的案例:
表一:中国研发药品License-out案例
既然药品领域的授权合作非常普遍,那么很容易想到的问题是,医疗器械领域这一模式是否适用呢?这一点,Licensing Consulting Group的CEO Rand Brenner先生认为答案是确定的。他的观点是:
医疗器械研发公司(尤其是小公司)至少有两个原因应积极将产品License-out给合作方:
1. 授权合作可使产品更快地进入目标市场,对于缺乏资源的小公司尤其如此。医疗器械在注册流程、监管环境、市场拓展方面都比较复杂,小公司通过授权大公司合作的方式,在目标市场可以更快的完成产品注册即市场准入。同时,大公司熟悉监管环境,降低了产品上市后面临的监管风险。大公司的品牌背书和渠道资源,其推广产品的速度绝非小公司能比。
2. 授权合作也是小公司一种自我保护的方式。小公司如果将产品授权给一个更大的公司来运作,大公司在专利方面的经验会保护产品的竞争安全性,延长产品的生命周期,这个能力通常是小公司不具备的。同时,大公司出于经济利益、公司声望乃至股价方面的考虑,会倾注更多的商业资源增加产品的销量,小公司可以获得的收益会远超出其独立运作产品。
现实中,授权方独立运作产品与授权其他公司合作并不矛盾,两者可以共存,在不同的市场、不同的领域、不同的时期采取不同的策略。
另一方面,从医疗器械产品引入方(资金实力雄厚的大型公司,或者风险资本支持的研发型公司)而言,也有如下两个原因促使他们有动力操作License-in:
1.大型公司传统的产品线拓展手段是公司收购。目前,标的公司的价格整体上偏高,导致收购后收益有限甚至没有收益。授权引入是一种折中办法,产品引入方发挥自己的专业优势,在目标产品阶段很早,价格还没有非常贵的阶段,买入授权,参与后续开发。这样降低了运作成本,提高了收益空间,同时也降低了开发风险。
2.大型公司很难快速响应市场,他们开发新产品的内部研发时间太长,又面临与现有产品线潜在冲突等复杂问题。医疗器械的创新通常是人或小公司解决工程问题,大公司及早发掘潜力产品,介入合作,不仅能够增加市场敏感度,同时也有利于疏导公司内部的利益矛盾等。
下面回到中国市场,为何在药品领域授权合作非常普遍,而在器械领域却很少呢?主要是由于如下几个原因:
创业团队国际化背景不足。中国近年来在药品领域出现较多顶尖教育及工作背景的海归回国创业,海外多年的工作及生活经历使得他们可以比较通畅地与国际顶尖公司进行授权合作。而中国医疗器械创业团队目前多脱身于国内大型器械公司,其强项是在某个技术或临床领域非常熟悉,能够快速推出KPI优于前就职公司的产品,在国内医院推广销售,但从事国际授权合作并没有相关积累。
产品的原创性及专利保护不足。相比于近年新药研发的如火如荼,中国的医疗器械在原创性上有所不足,很难见到能在国际市场上亮眼的产品,国际巨头有些“看不上”。加之,法律方面人才匮乏,专利保护不足,而这对进行国际授权合作是至关重要的。
产品市场空间不足。大部分医疗器械的市场天花板比较低,不像药品,动辄数十亿美元的市场。而如果市场空间本身有限,这个产品对于国际巨头是缺乏授权合作动力的。
综上观点,中国医疗器械产品如果想授权给海外巨头公司,必须是条件是:团队具有国际视野,能够无障碍国际合作,甚至在国外具有一定知名度;产品具有国际级的原创性,以至于巨头公司认为授权引入比独立开发更具吸引力,同时,应在专利方面足够严谨没有瑕疵;市场空间足够大,对引入方自身的产品线来讲具有足够的影响力。
尽管中国医疗器械的授权合作目前还很少,但市场上还是出现了代表性的案例。
License-in代表案例:再鼎医药从Novocure引入肿瘤电场治疗器械Optune®
再鼎医药于2018年9月从Novocure授权引进了肿瘤治疗电场(Tumor Treating Fields,简称TTF,商品名Optune®)技术,目前已经在美国、欧洲、日本等国上市用于治疗GBM,并在同步进行多项实体肿瘤适应症的临床试验。
在肿瘤细胞分裂增殖的过程中,有很多蛋白质参与,这些蛋白质有的会带电,为了保证细胞分裂正常进行,这些带电的蛋白质在肿瘤细胞里面呈规则分布。体外和体内研究已经证实,Optune®能够在肿瘤细胞内部形成低强度的交流电场,对携带电荷的细胞成分施加物理力,从而干扰肿瘤细胞的分裂和复制过程,使受电场影响的癌细胞死亡,从而延缓和逆转肿瘤生长。
Optune®作为一种新型、无创的肿瘤治疗方式,在胶质母细胞瘤的治疗上展现出卓越的疗效,国际著名癌症期刊《Clinical Cancer Research》指出,肿瘤治疗电场被称为手术、放疗、化疗和免疫/靶向治疗之外的"第四种治疗形式"。香港是继美国、欧洲和日本之后第四个上市该治疗方案的市场。
